Publicado: 18/12/19 11:53 Categorías: Biología molecular
¿Puede el editado del genoma ayudar a combatir el VIH?
El pasado 1 de diciembre se conmemoró el Día Internacional de la Acción contra el SIDA, una enfermedad que continúa afectando a millones de personas. Bajo el lema “Las comunidades marcan la diferencia”, el objetivo principal de la campaña llevada a cabo este año es concienciar sobre la importancia del papel que juegan las distintas asociaciones de personas en la lucha contra esta enfermedad.
El VIH, también conocido como Virus de la Inmunodeficiencia Humana, es un retrovirus que ataca y destruye a los linfocitos T CD4+ del sistema inmune, uno de los tipos celulares más implicados en la defensa del organismo. De este modo, sin un tratamiento adecuado, la infección por VIH es capaz de colonizar y deteriorar dicho organismo hasta el punto de que éste no sea capaz de hacer frente a ninguna enfermedad. Es este estadio el que se conoce como SIDA, o Síndrome de Inmunodeficiencia Adquirida.
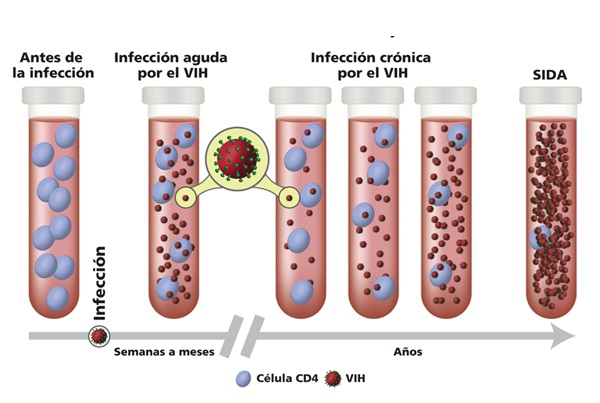
De aquí la importancia de la detección y el tratamiento temprano con fármacos antirretrovirales, que permitan la cronificación de la enfermedad y, con ello, la funcionalidad continuada del sistema inmunitario.
Son muchos los estudios e investigaciones que se desarrollan en relación a esta enfermedad; de hecho, este 2019 ha sido un año especialmente fructífero en la lucha contra el virus, pues se han producido múltiples avances tanto a nivel diagnóstico como curativo.
Uno de los más importantes ha sido, sin duda, el caso de un paciente en el que se ha logrado erradicar el VIH por completo tras someterse a un trasplante de células madre para tratar un linfoma. Se trata de la segunda curación completa de esta enfermedad, pues ya en el año 2007 ocurrió otro hecho similar.
La clave en ambos casos es la presencia de una mutación en las células CD4+ del donante, concretamente en la proteína CCR5, que forma parte de la membrana de los linfocitos. Dicha proteína es vital para la unión y posterior infección de las células por el VIH, por lo que su inactivación (por mutaciones como la CCR5 Delta 32) impide la entrada del virus.
Todo esto ha sido de gran ayuda para identificar una potencial diana en la lucha contra el SIDA, la proteína CCR5. Sin embargo, el trasplante de médula ósea no está exento de riesgos, por lo que no resulta una estrategia terapéutica factible en aquellos casos de VIH en los que la infección se controle con antirretrovirales.
Actualmente, los esfuerzos de los investigadores se centran en una estrategia distinta basada en la terapia génica. De este modo, se podrían extraer las células madre de los pacientes infectados, editarlas en el laboratorio para inactivar CCR5 y volver a infundirlas; todo ello sin necesidad de modificar la línea germinal.
La aplicación de técnicas como CRISPR/Cas lleva ya años siendo testada en el laboratorio tanto en líneas celulares como en animales, pero no ha sido hasta este año cuando se ha aplicado por primera vez en seres humanos.
Así, investigadores de China han publicado recientemente los primeros resultados de la utilización de este sistema para tratar el VIH en humanos. Se trata de un paciente infectado que padecía de leucemia linfoblástica aguda al que se le realizó un trasplante de células madre previamente editadas en el laboratorio para modificar el gen que codifica CCR5. Tras el tratamiento, el cáncer remitió por completo; sin embargo, el reemplazo de los linfocitos modificados frente al total (5%-8%) no fue suficiente para alcanzar efecto terapéutico en relación al VIH.
De todos modos, estos resultados han sido de gran utilidad, al servir tanto para validar la seguridad del empleo de la tecnología CRISPR en el ámbito clínico como para sentar las bases que permitan continuar las investigaciones al respecto. Ahora, el foco debe ponerse en la mejora del rendimiento de la técnica, de modo que puedan alcanzarse proporciones de edición mayores.
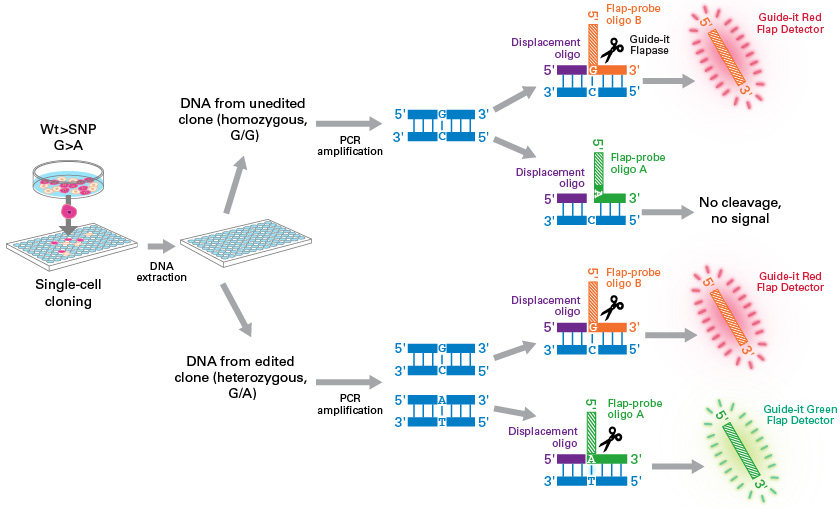
¿Y tú, trabajas con CRISPR? Descubre el nuevo “Guide-it Knockin Screening Kit” de Takara y optimiza al máximo el proceso de detección e identificación de la edición.
Con un protocolo sencillo y en menos de 4 horas, este producto te permite localizar tus mutaciones o inserciones de interés en ambos alelos de cualquier gen, tanto en poblaciones heterogéneas como en colonias clonales.
El método se basa en una amplificación inicial del target site de interés (mediante PCR) seguida de un ensayo enzimático dual-color. Además, con el fin de facilitar al máximo la labor del investigador, Takara pone a tu disposición una completa herramienta online para el diseño de los primers necesarios para la ejecución del ensayo.
Referencia:
Xu L, et al. CRISPR-Edited Stem Cells in a Patient with HIV and Acute Lymphocytic Leukemia. NEJM. 2019.

 El poder del RNA: de la ciencia básica a las terapias de precisión
El poder del RNA: de la ciencia básica a las terapias de precisión
 La microbiología cambia de color: La permanencia de los medios cromogénicos
La microbiología cambia de color: La permanencia de los medios cromogénicos
 Probióticos: ¿Cuál es el bueno?
Probióticos: ¿Cuál es el bueno?
 Virus recombinantes en investigación y bioproducción: retos y soluciones
Virus recombinantes en investigación y bioproducción: retos y soluciones
 Condalab y BD: una colaboración que impulsa las ómicas espaciales
Condalab y BD: una colaboración que impulsa las ómicas espaciales